2022/10/26
カイオムニュースレター(Vol.8)
Tribody™を用いた新規がん免疫療法薬創製に関する論文が掲載されました
~当社の多重特異性抗体Tribody™を用いた研究成果がJournal of Experimental & Clinical Cancer Research誌に掲載されました~
当社の多重特異性抗体Tribody™による新規がん治療薬の創製を目指して、当社がイタリアの公的研究機関Ceinge-Biotecnologie Avanzate(以下、Ceinge)と行ったがん免疫療法に関する共同研究の成果が、国際的な学術雑誌であるJournal of Experimental & Clinical Cancer Research誌に掲載されました。
Tribody技術は、通常は一つの標的しか認識することができない抗体を改変して、一つの抗体分子が複数の異なる標的に結合できるようにした多重特異性抗体(二つの抗原に結合するバイスペシフィック抗体や、さらに抗原結合部位を増やしたマルチスペシフィック抗体)を創出する技術です。バイスペシフィック抗体・マルチスペシフィック抗体を用いた次世代型の抗体医薬品開発は、全世界的に非常に盛んに取り組まれており、数多くの薬剤が臨床開発されています。当社においてもTribody™により創製した多重特異性抗体であるCBA-1535の臨床第1相試験を進めています。
<共同研究成果の概要>
本共同研究では、がん治療用抗体として当社が臨床開発を行っているTb535H(CBA-1535)をベースに、さらに「免疫チェックポイント阻害」機能を導入したTribody™を構築しました(53X型Tribody™)。53X型Tribody™は、Tb535Hよりも強力な抗腫瘍活性を示し、特に5T4×CD3×PD-L1(53L10型)の組み合わせにおいて最も強い腫瘍増殖抑制効果を発揮することを示しました。
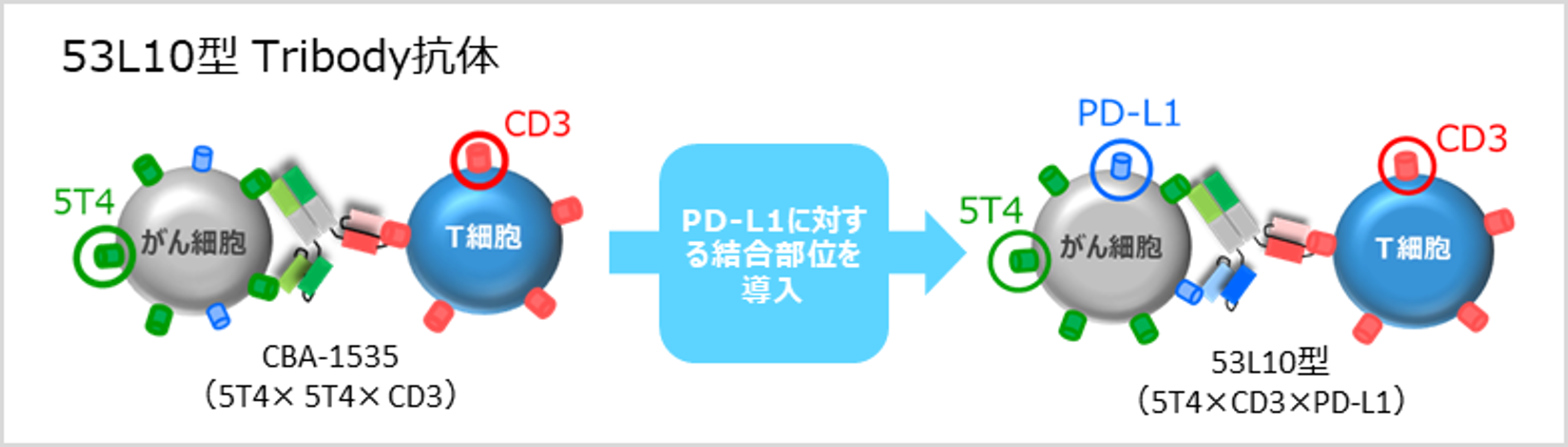
<免疫チェックポイントについて>
PD-L1という分子は、免疫チェックポイントという仕組みに関与する分子の一つで、がん細胞はこれを悪用することによって、免疫細胞の攻撃から逃れます。がん細胞上にあるPD-L1がT細胞(免疫細胞)上のPD-1という分子に結合すると、T細胞の働きにブレーキがかかり、がん細胞への攻撃が阻止されてしまいます。PD-1/PD-L1のような免疫チェックポイント関連分子の結合を阻害して、免疫系ががんを攻撃できるようにする薬剤を免疫チェックポイント阻害剤といい、オプジーボやキイトルーダ、ヤーボイなどがすでに広く使われ、高い治療効果をあげています。
<研究概要>
本研究では、Tb535HをベースにPD-L1結合抗体を導入した53L10型Tribodyの他にPD-1やLAG-3などの免疫チェックポイント分子の結合阻害抗体を導入した53X型Tribody(「5T4×CD3×PD-1(53D型)」、「5T4×CD3×LAG-3(53G型)」等)を構築し、in vitroでのT細胞の活性化やがん細胞に対する殺細胞活性、in vivoでの腫瘍退縮効果などを検証しました。
<肺がんモデルマウス薬効データの紹介>
Tb535H投与群(20µg/マウス)において、PBS(リン酸緩衝生理食塩水)を投与した群と比較して有意な腫瘍増殖抑制があることが観察されましたが、低用量(2μg/マウス)群では腫瘍増殖抑制は認められませんでした。(グラフA参照) 一方で、53L1(20µg/マウス)の抗腫瘍活性は、同量のTb535Hと比較して有意に増強され、(グラフB参照)、53L10投与群においては、2µg/マウスおよび20µg/マウスのいずれの用量でも、PBS投与群と比較して、有意な腫瘍増殖抑制効果が観察されました。
具体的には、53L10(2µg/マウス)投与群において、投与開始から50日目の腫瘍増殖抑制率はPBS投与群と比較して41.5%に達し、53L10の高用量投与群(20µg/マウス)においては100%の腫瘍増殖抑制率が観察されました。さらに、53L10(20µg/マウス)投与群では、試験最終日(50日目)において、すべてのマウスで完全な腫瘍退縮が認められました。(グラフC参照)
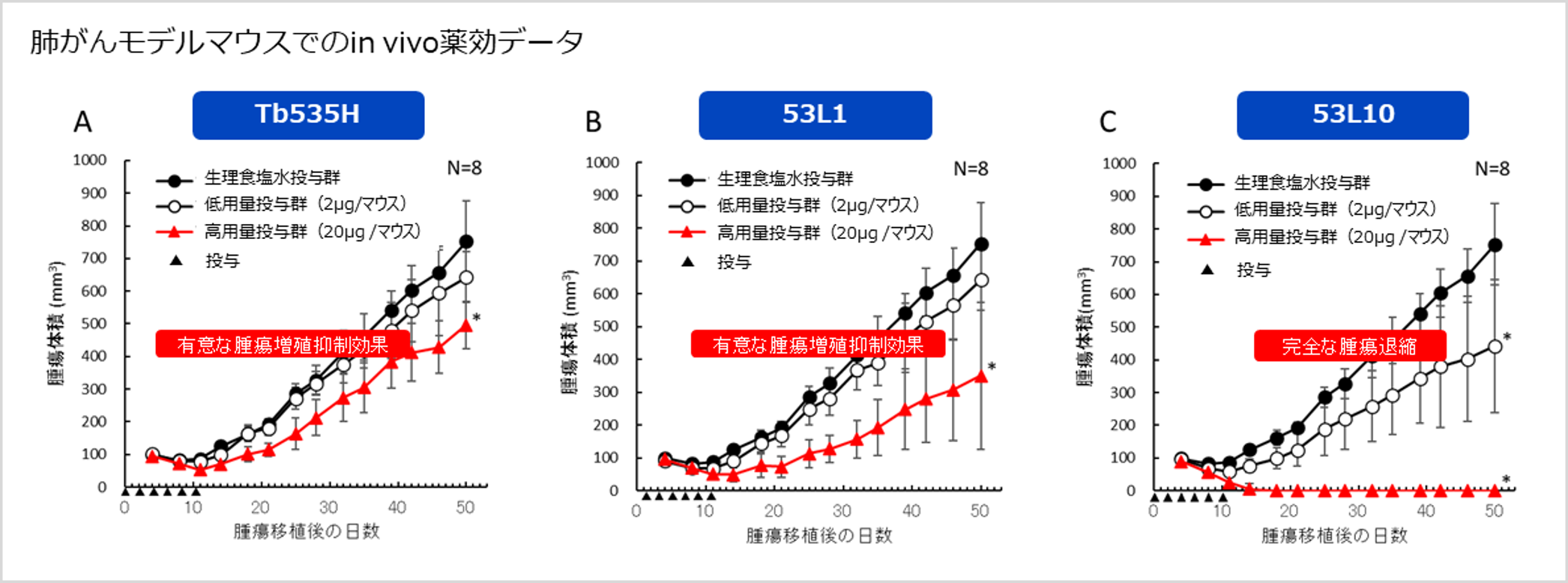
この実験においては、Tb535H、53L1型、および53L10型投与群のいずれの群でも腫瘍増殖抑制効果が認められておりますが、特に53L10型(20µg/マウス)投与群においては完全な腫瘍退縮が観られるなど非常に強い抗腫瘍活性が認められています。
<今後について>
当社が臨床第1相試験を進めているTb535Hは、T細胞の増殖と活性化を誘導してがん細胞に対する強力な細胞傷害活性を発揮することが期待されるがん治療用抗体ですが、本共同研究で構築した53L1型や53L10型は、Tb535Hにさらに免疫チェックポイント阻害の機能を持たせることにより、より強力な治療効果の発揮を期待するものです。
当社では本共同研究によって得られた成果について特許出願を完了しており、特に53L10型Tribody™はプロジェクト名をPTRYとし、今後の当社創薬パイプラインとして研究開発、事業化を推進してまいります。当社が現在進めているPCDCやCBA-1205の導出活動の中でも、CBA-1535やPTRYに関する問い合わせや質問についても得る機会が多くあります。本論文データも活用しながら着実に事業化にむけて進めてまいります。
<Ceinge-Biotecnologie Avanzateについて>
Ceingeは1983年に設立されたナポリにある公的研究機関です。Ceingeは、人類の健康に特化した分子生物学や先進バイオテクノロジーの分野で活動しており、遺伝病の研究、診断の分野でイタリア国内外において優秀な業績を残しています。
【発表雑誌】
雑誌名: Journal of Experimental & Clinical Cancer Research
論文タイトル: “Novel Tri-Specific Tribodies induce strong T Cell Activation and anti-Tumor effects in vitro and in vivo”
著者:Margherita Passariello, Asami Yoshioka, Kota Takahashi, Shu-ichi Hashimoto, Toshikazu Inoue, Koji Nakamura and Claudia De Lorenzo
論文全文URL:https://doi.org/10.1186/s13046-022-02474-3

<免疫チェックポイント阻害薬とは>
T細胞(免疫細胞)には、がん細胞などの異常な細胞を見つけて攻撃する機能があります。(図1)
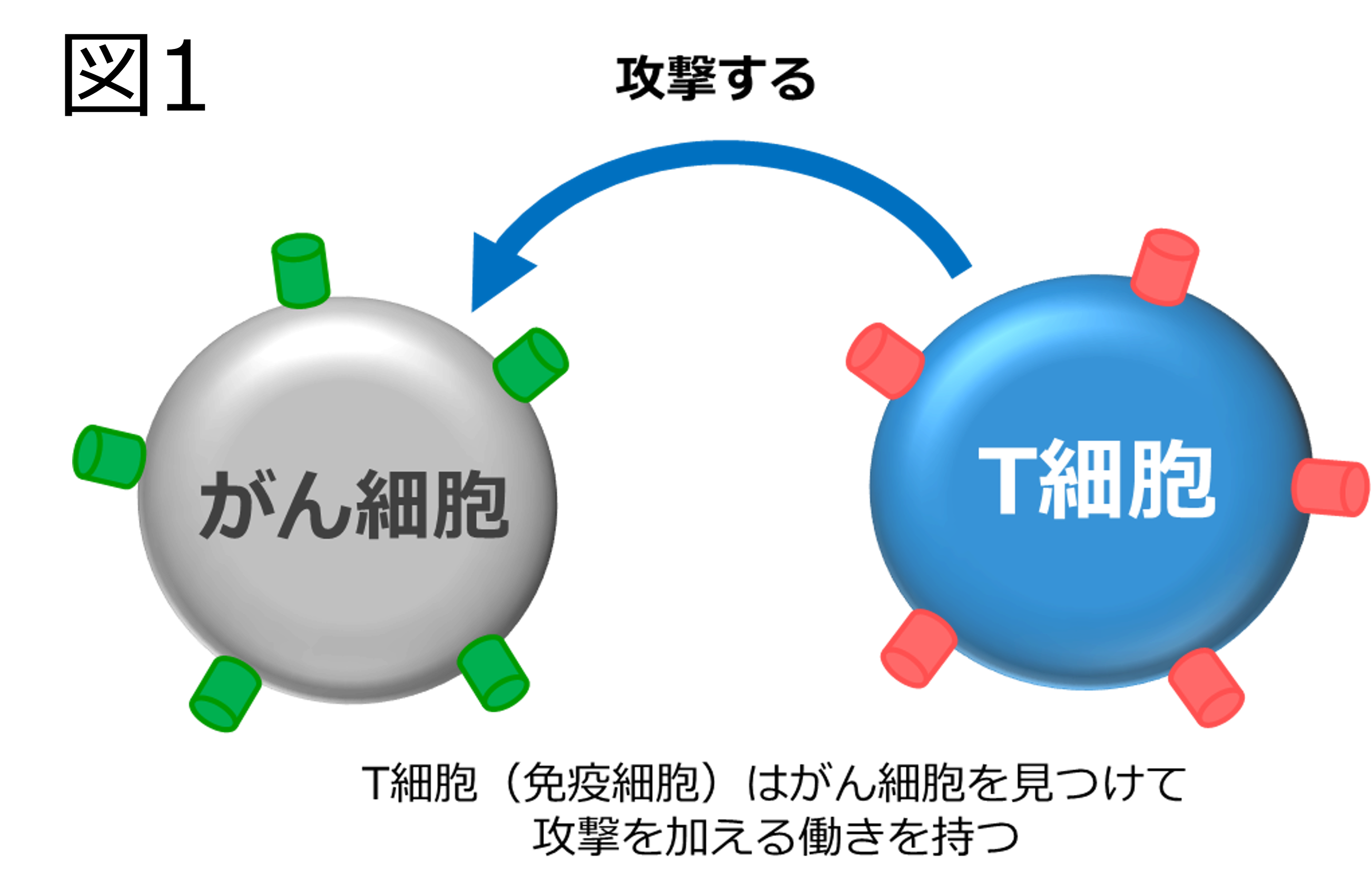
同時に、T細胞には免疫系が過剰に働いて正常な細胞を攻撃することがないよう、その働きを抑制するシステムも備わっています。がん細胞はこの仕組みを悪用して免疫細胞の攻撃から逃れます。たとえばT細胞上のPD-1という分子に、がん細胞表面に発現しているPD-L1が結合すると、T細胞の働きにブレーキがかかり、がん細胞への攻撃が阻止されます。(図2)
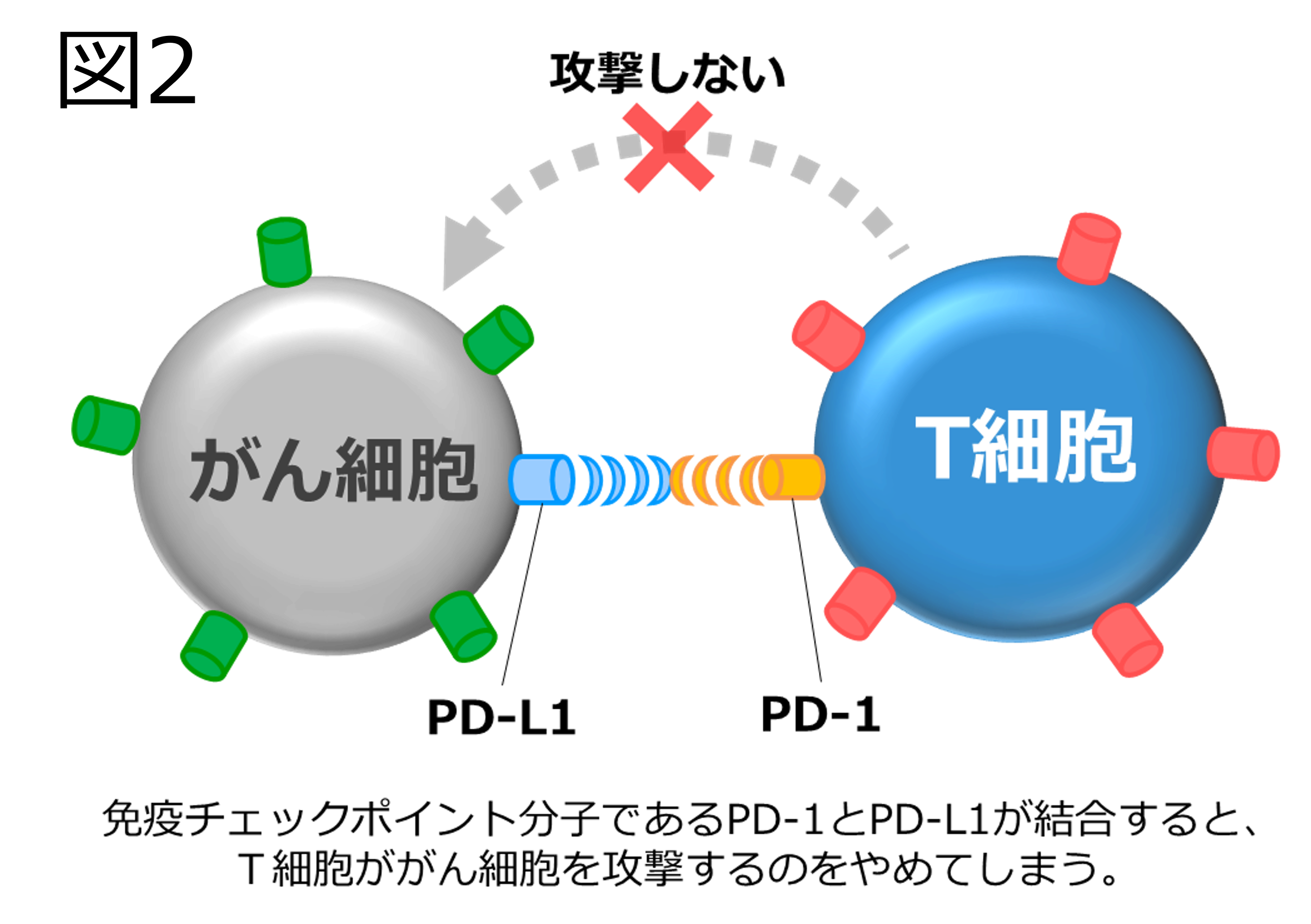
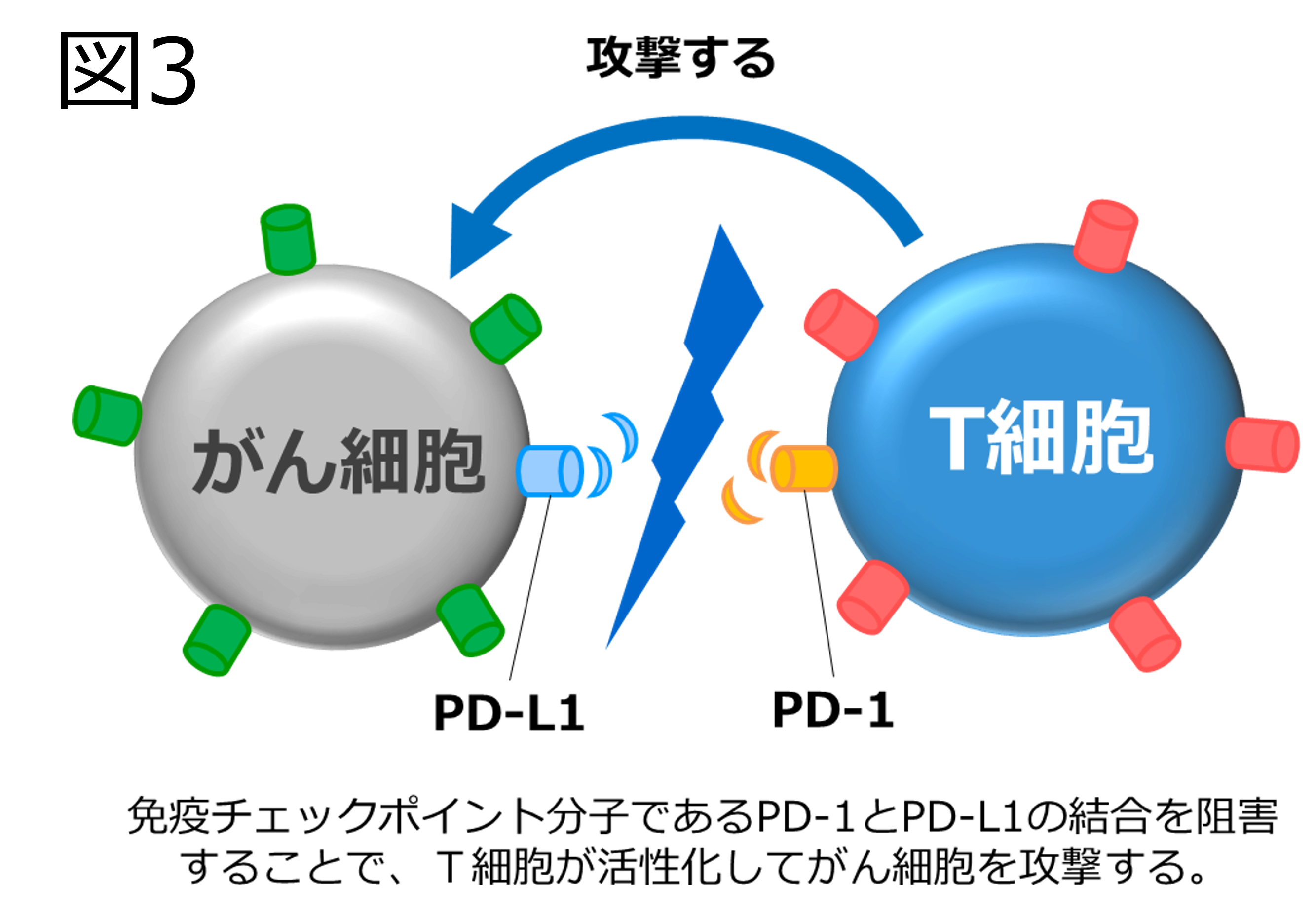
PD-1とPD-L1の結合を阻害することで、T細胞の働きを再び活性化してがん細胞を攻撃します。(図3)
免疫チェックポイント分子としてPD-1/PD-L1のほかにも多くの分子が知られており、また、免疫チェックポイント阻害の機序も複数の方法があります。がんの三大標準治療と言われてきた外科手術、薬物療法、放射線治療に続く、第4のがん治療法として注目されるがん免疫療法は、人が本来持っている免疫力を活用する治療法として研究開発が盛んにおこなわれています。





